α 就像一个跷跷板的支点,一头连着基因表达,一头连着空间结构。你想要哪头更重要,就往哪头拨一下。实际操作中,如果没有特别明确的先验知识,可以先用个折中的值,比如0.5,跑一遍看看结果。然后,根据结果,再慢慢调整。如果发现整合后的结果,细胞都挤在一起,分不清彼此,那可能就需要降低 α,让基因表达来发挥更大的作用;反之,如果细胞分布过于分散,失去了空间上的连续性,那就可能需要提高 α,让空间结构来约束它们。
总之,α 的选择没有一个固定的答案,需要不断尝试和调整,才能找到最适合你的数据的那个“甜蜜点”。
SIMO算法在疾病研究和治疗策略开发方面的潜力那是大大的!文章里提到了小鼠皮层和人类心肌梗死,这只是冰山一角。实际上,SIMO可以应用在任何涉及复杂组织微环境和多组学数据的疾病研究中。
1. 肿瘤研究:肿瘤的发生发展受到肿瘤细胞和周围微环境的共同影响。肿瘤微环境包含多种细胞类型(如免疫细胞、血管内皮细胞、成纤维细胞等),以及复杂的细胞间互作网络。利用SIMO可以整合肿瘤组织的多组学数据(如基因组、转录组、蛋白质组、代谢组等),重构肿瘤微环境的空间结构,鉴定关键的细胞互作和信号通路,发现潜在的治疗靶点。
2. 神经退行性疾病研究:阿尔茨海默病、帕金森病等神经退行性疾病的病理机制复杂,涉及多种细胞类型(如神经元、胶质细胞、免疫细胞等)和分子通路。利用SIMO可以整合患者脑组织的多组学数据,研究疾病进展过程中细胞类型组成、基因表达谱和空间分布的变化,揭示疾病的病理机制,寻找潜在的治疗靶点。
3. 自身免疫性疾病研究:类风湿性关节炎、系统性红斑狼疮等自身免疫性疾病的发生与免疫系统的异常激活有关。利用SIMO可以整合患者病变组织(如关节滑膜、皮肤等)的多组学数据,研究免疫细胞的类型、状态和空间分布,揭示疾病的免疫病理机制,为开发更精准的免疫治疗策略提供依据。
总而言之,只要是涉及到复杂组织微环境和多组学数据的疾病研究,SIMO都有用武之地。
SIMO 的应用前景非常广阔,以下是一些可能的研究方向:
* 药物研发:可以利用 SIMO 分析药物在体内的分布和作用机制,优化药物设计和给药方案。
* 再生医学:可以利用 SIMO 研究组织再生过程中的细胞行为和分子调控,促进组织修复和器官再生。
* 衰老研究:可以利用 SIMO 研究衰老过程中组织结构和细胞功能的变化,寻找延缓衰老的干预措施。
此外,SIMO 还可以与其他技术结合,例如单细胞基因编辑、CRISPR 筛选等,进一步扩展其应用范围。
SIMO 的妙处在于它没有强行把所有类型的数据“捏”在一起,而是采取了一种更聪明的策略,也就是文中所说的“分步对齐”。你可以把它想象成一个翻译的过程,不同类型的组学数据就像不同的语言,SIMO 需要找到一个共同的“翻译器”才能把它们联系起来。对于转录组数据,这个“翻译器”就是基因表达本身;对于非转录组数据,SIMO 会寻找与转录组数据相关的特征,比如基因活性分数,作为连接不同组学数据的桥梁。
此外,SIMO 还使用了最优传输算法,这种算法可以找到不同组学数据之间最佳的“匹配”方式,使得整合后的结果既能反映数据的相似性,又能保留数据的独特性。更重要的是,SIMO 在整合的过程中会考虑到空间信息,这使得整合后的结果更具有生物学意义,因为细胞的类型和功能往往与其所处的空间位置密切相关。
当然,SIMO 也不是万能的。在处理某些特殊的组学数据时,可能需要根据数据的特点进行调整,才能获得最佳的整合效果。
SIMO算法里,α这个超参数其实扮演着一个“平衡器”的角色。它用来平衡基因表达相似性和空间结构的相似性。α值如果设置得比较小,比如接近0,模型就会更看重细胞和斑点在转录组层面的相似度,说白了就是“英雄所见略同,基因表达一致”。但如果α值设置得比较大,比如接近1,模型就会更关注细胞和斑点在空间图里的相对位置和连接关系,也就是“远亲不如近邻,空间位置很重要”。
实际应用中,α值的选择就得根据具体的数据集和研究目的来定了。如果你的数据集质量很高,基因表达信息很可靠,那就可以把α设置得小一点,让模型更多地参考基因表达信息。但如果你的数据集里噪音比较多,空间信息相对更可靠,那就应该把α设置得大一点,让模型更多地参考空间信息。通常来说,文章里说 α 设为 0.1 时效果最好,可能是一个普适性的经验值,但最好还是根据实际情况进行调整。
更严谨的做法是,可以尝试不同的α值,然后通过一些评价指标(比如整合后的细胞类型分布是否合理,或者某些已知marker基因的空间表达模式是否符合预期)来评估整合效果,最终选择一个最优的α值。
SIMO 在疾病研究领域绝对是一把利器!除了文章中提到的案例,我还能想到以下几个应用场景:
* 自身免疫疾病:比如类风湿性关节炎,SIMO 可以帮助我们理解关节滑膜中不同细胞类型的空间分布,以及它们之间的相互作用,从而找到更有效的治疗靶点。
* 感染性疾病:在研究病毒感染时,SIMO 可以帮助我们了解病毒在组织中的传播路径,以及免疫细胞对病毒的反应,从而开发出更精准的抗病毒策略。
* 器官移植:SIMO 可以帮助我们评估移植器官的质量,预测移植后的排异反应,从而提高移植的成功率。
总之,只要是涉及到复杂组织结构和多种分子机制的疾病,SIMO 都有潜力发挥重要作用。当然,这还需要研究者们不断地探索和实践。
保证整合的准确性和生物学意义,关键在于找到不同组学数据之间的内在联系。SIMO 通过以下几个方面来做到这一点:
* 数据预处理:对不同类型的组学数据进行标准化和归一化处理,消除技术误差带来的影响。
* 特征选择:选择与研究问题相关的关键特征,例如差异表达基因、显著变化的染色质区域等。
* 模态间关联:利用已知的生物学知识,建立不同组学数据之间的关联。例如,基因表达与基因调控区域的开放程度之间存在关联。
* 空间信息整合:将空间位置信息纳入整合过程,考虑到细胞之间的空间关系。
此外,还需要对整合结果进行验证,例如与已知的生物学通路、细胞类型marker基因等进行比较,确保整合结果具有生物学意义。
从技术角度讲,SIMO 中的 α 参数是融合 Gromov-Wasserstein 最优传输过程中基因表达相似性和图结构相似性的权重。当 α 接近 0 时,整合过程会更加依赖基因表达的相似性,这在转录组数据质量较高的情况下可能更有效。反之,当 α 接近 1 时,整合过程会更加侧重于空间图的结构相似性,这对于空间信息更为关键的情况可能更有利。
选择合适的 α 值需要根据具体实验数据和整合目标进行调整。一种常用的方法是通过交叉验证,即在不同的 α 值下进行多次整合,并评估整合结果的准确性和稳定性。此外,可以利用已知的生物学知识作为指导,例如,如果已知某些细胞类型在空间上具有特定的分布模式,则可以调整 α 值,使得整合结果能够更好地反映这些模式。
另外,还可以考虑使用自动化参数优化方法,例如网格搜索或贝叶斯优化,来寻找最佳的 α 值。这些方法可以系统地探索不同的参数组合,并基于预定义的评估指标(如整合准确性、细胞类型分离度等)来选择最优的参数配置。
SIMO算法在处理不同类型的组学数据时,为了保证整合的准确性和生物学意义,主要采取了以下几个策略:
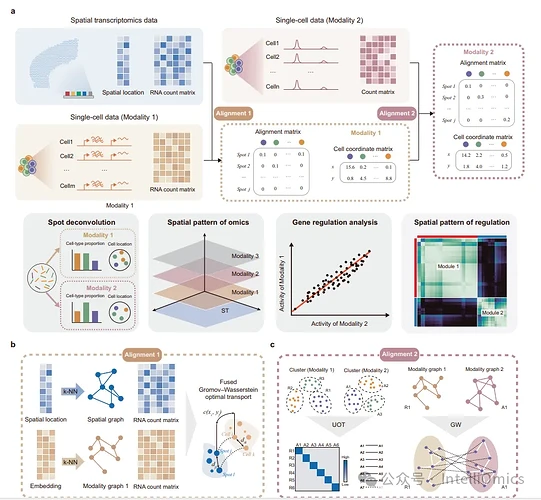
1. 分步对齐策略:SIMO没有直接将所有组学数据一股脑地整合在一起,而是采用了一种“各个击破”的分步策略。它首先整合空间转录组数据和单细胞RNA测序数据,因为这两者都反映了转录组层面的信息,具有天然的联系。然后再将其他非转录组数据(如ATAC-seq数据)与scRNA-seq数据进行整合。这种分步策略降低了整合的复杂性,也更容易保证整合的准确性。
2. 桥梁作用:在整合不同类型的组学数据时,SIMO会寻找一个共同的“桥梁”,将它们联系起来。比如,在整合RNA和ATAC数据时,SIMO使用了基因活性分数作为桥梁,通过计算基因表达和基因活性分数之间的相关性,来建立不同模态数据之间的联系。这种方法能够有效地利用不同组学数据之间的内在联系,提高整合的生物学意义。
3. 非平衡最优传输:在模态间的标签转移时,SIMO采用了非平衡最优传输算法。这种算法允许不同模态之间存在细胞数量上的差异,更加符合实际情况。
总的来说,SIMO算法通过精巧的设计,保证了在整合不同类型的组学数据时,既能保证整合的准确性,又能最大限度地保留生物学意义。